
Нажалост, навикли смо да слушамо о различитим врстама деменција али обично нам није јасно објашњено шта се дешава са мозгом када патимо од ових болести. Из тог разлога је циљ нашег данашњег чланка да на најједноставнији могући начин објаснимо шта се дешава са нашим мозгом када нам се дијагностикује Алцхајмерова болест.
Такође ћемо разговарати о једном од напретка у лечењу Алцхајмерове болести који највише надају. Ово ново откриће је недавно објављено у часопису Природа толико је важно да би добијени резултати могли да промене ток ове болести какву данас познајемо.
Мозак и Алцхајмерова болест
Када болујете од Алцхајмерове болести, долази до тешке дегенерације мозга посебно хипокампуса енторхиналног кортекса неокортекса (посебно области које повезује фронтални и темпорални режањ) базалних ганглија лоцус цоерулеуса и језгара рапхе.
Међутим, на шта се све ово односи? јесмо учење управљање памћењем и емоцијама. Као што видите, све ове функције су веома угрожене код пацијената који пате од Алцхајмерове болести.
А како се одвија дегенерација ових простора? То је због развоја сенилних плакова или амилоидних плакова и неурофибриларних кластера . Међутим, пре него што објасните шта су ови плакови или кластери, важно је знати од чега се састоје неурони:
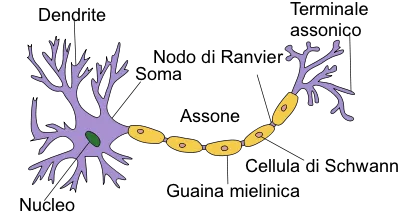
- Сома: то је централно тело неурона у коме се налази његово језгро и све информације које прима од других неурона који га окружују.
- Аксон: ово је највећа избочина која излази из соме и која служи за слање информација неурона свим осталим неуронима.
- Дендрити: то су мале екстензије које излазе из централног тела неурона и које примају информације од других неурона.
Сенилни плакови су наслаге које се налазе изван можданих ћелија и састоје се од језгра чији је протеин познат као бета-амилоид . Ове наслаге су окружене аксонима и дендритима који су у процесу дегенерације. Ова дегенерација је природан процес у сваком људском мозгу и стога није патолошка.
У близини сенилних плакова налазимо и микроглиоцити активни и астроцити реактивне ћелије укључене у уништавање других штетних. Такозване фагоцитне глијалне ћелије такође интервенишу и уништавају аксоне и дегенерисане дендрите остављајући само бета-амилоидно језгро.
Нуерофибриларни кластери се састоје од умирућег неурона који садржи међућелијску акумулацију испреплетених ланаца тау протеина . Нормални тау протеин је супстанца микротубула која представља ћелијски транспортни механизам.
Током развоја Алцхајмерове болести
Ови јони такође мењају транспорт супстанци унутар ћелије која затим умире и оставља масу протеинских филамената на свом месту.
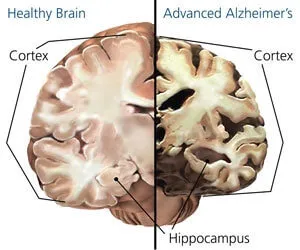
Чекај, да ли смо управо рекли да неурони пропадају? Да, тако је и то је природан процес људског старења. Међутим, у случају Алцхајмерове болести, формирање амилоидних плакова је последица производње дефектног облика бета-амилоида који убрзава смрт неурона, што разликује процес од нормалног старења.
То значи да у погледу пластичност да сви мозгови имају у којима постоје неурони који дегенеришу али не изазивају никаква оштећења или који су замењени другим, долази до промене овог процеса због бета-амилоидних плакова.
Важност новог третмана за Алцхајмерову болест
Недавно часопис Природа објавио чланак под насловом Алцхајмерова болест: Напад на амилоид-β протеин написао Ериц М. Реиман са неким сарадницима. Овај чланак објашњава откриће новог напретка у лечењу Алцхајмерове болести, посебно на тему бета-амилоидног протеина.
Истраживање Реимана и његових сарадника се фокусира на нови лек који спречава уништавање неурона и накупљање амилоидних протеинских плакова који се као што смо раније објаснили сматрају једним од главних узрока когнитивног погоршања код Алцхајмерове болести.
Феликс Вињуела, неуролог и истраживач у болници Вирген Макарена у Севиљи, у Шпанији, изјавио је да овај лек стиже до мозга, спаја се са депозитом токсичних супстанци и одатле га елиминише. Штавише, могли смо да видимо да је већа количина примењеног лека једнака бољем опоравку пацијената.
Међутим, исти истраживачи подвлаче да је за сада реч о истраживању спроведеном у 300 болница у Северној Америци, Европи и Азији, посебно на пацијентима који пате од благог когнитивног оштећења (МЦИ) и да иако је ово напредак који даје велике наде, још је дуг пут до његовог коришћења и док се његови позитивни дугорочни ефекти не могу показати.















